L'immunothérapie représente aujourd'hui une révolution médicale majeure dans la lutte contre le cancer. Contrairement aux traitements classiques qui attaquent directement les tumeurs, cette approche novatrice mobilise votre propre système immunitaire pour combattre la maladie. Les résultats sont impressionnants : des patients autrefois condamnés retrouvent espoir grâce à des taux de survie considérablement améliorés. Des mélanomes aux leucémies, ces nouvelles thérapies transforment radicalement le pronostic de nombreux cancers.
Les avancées récentes dans ce domaine bouleversent les standards de soins oncologiques. Des anticorps révolutionnaires réveillent vos défenses naturelles, tandis que des cellules reprogrammées détruisent les tumeurs avec une précision chirurgicale. Par ailleurs, des vaccins personnalisés adaptés à votre profil génétique ouvrent des perspectives inédites. Les virus modifiés s'attaquent désormais sélectivement aux cellules cancéreuses, et les combinaisons thérapeutiques multiplient l'efficacité des traitements. Découvrez comment ces cinq innovations majeures redéfinissent les possibilités thérapeutiques et offrent un nouvel horizon aux patients atteints de cancer. Votre santé mérite ces avancées scientifiques exceptionnelles.
Les inhibiteurs de points de contrôle immunitaire révolutionnent le traitement du mélanome
Le mélanome représentait autrefois l'un des cancers les plus redoutés, avec un pronostic particulièrement sombre aux stades avancés. Cependant, l'arrivée des inhibiteurs de points de contrôle immunitaire a complètement transformé la prise en charge de cette maladie. Ces molécules innovantes permettent de débloquer le système immunitaire pour qu'il reconnaisse et attaque efficacement les cellules cancéreuses. Avant leur apparition, les options thérapeutiques restaient limitées et la survie à cinq ans dépassait rarement 10% pour les mélanomes métastatiques. Désormais, plus de 50% des patients traités avec ces immunothérapies vivent au-delà de cette échéance.
Comment les anticorps anti-PD-1 et anti-CTLA-4 réactivent les défenses naturelles
Les anticorps anti-PD-1 comme le nivolumab et le pembrolizumab agissent en bloquant une protéine située à la surface des lymphocytes T. Cette protéine, appelée PD-1, fonctionne normalement comme un frein qui empêche le système immunitaire de s'emballer. Malheureusement, les cellules tumorales exploitent ce mécanisme en produisant des ligands qui activent ce frein, rendant ainsi les lymphocytes T inactifs. D'autre part, les anticorps anti-CTLA-4 tels que l'ipilimumab ciblent un autre point de contrôle situé plus en amont du processus immunitaire. Par conséquent, ces deux types d'anticorps libèrent les défenses naturelles de l'organisme en désactivant ces freins moléculaires. Les résultats cliniques montrent des réponses durables chez de nombreux patients, avec des tumeurs qui régressent parfois complètement. De plus, la combinaison de ces deux approches offre des taux de réponse encore plus impressionnants, bien qu'elle s'accompagne d'effets secondaires plus marqués.
Mécanismes moléculaires de déblocage des lymphocytes T contre les cellules tumorales
Au niveau moléculaire, le déblocage des lymphocytes T repose sur plusieurs étapes précises. D'abord, les anticorps thérapeutiques se fixent sur les récepteurs PD-1 ou CTLA-4 présents à la surface des lymphocytes. Ensuite, cette liaison empêche l'interaction entre ces récepteurs et leurs ligands produits par les cellules tumorales ou les cellules présentatrices d'antigènes. Finalement, les lymphocytes T retrouvent leur capacité à proliférer, à produire des cytokines inflammatoires et à détruire directement les cellules cancéreuses. Les principaux avantages de cette approche incluent :
- Une activation durable du système immunitaire qui peut maintenir son effet après l'arrêt du traitement
- La possibilité de traiter des métastases multiples simultanément grâce à une réponse systémique
- Une mémoire immunitaire qui protège contre les récidives à long terme
- Des effets bénéfiques observés même chez des patients précédemment traités sans succès
Néanmoins, tous les patients ne répondent pas à ces traitements, ce qui pousse les chercheurs à identifier des biomarqueurs prédictifs pour mieux sélectionner les candidats idéaux.
Les thérapies CAR-T offrent de nouveaux espoirs face aux leucémies et lymphomes
Les thérapies CAR-T représentent une révolution majeure dans le traitement des cancers du sang. Cette approche innovante consiste à prélever les propres cellules immunitaires du patient, à les modifier génétiquement en laboratoire, puis à les réinjecter pour qu'elles attaquent spécifiquement les cellules cancéreuses. Contrairement aux traitements conventionnels, cette méthode transforme le système immunitaire du patient en une arme personnalisée contre le cancer. Les résultats obtenus dépassent largement les attentes initiales des chercheurs.

- Thérapie révolutionnaire utilisant les cellules du patient reprogrammées contre le cancer
La reprogrammation génétique des cellules immunitaires pour cibler le cancer
Le processus de création des cellules CAR-T repose sur une ingénierie génétique sophistiquée. Les lymphocytes T du patient sont d'abord collectés par aphérèse, une technique qui permet de séparer les différents composants du sang. Ensuite, ces cellules subissent une modification génétique qui leur ajoute un récepteur chimérique antigénique, d'où le nom CAR-T. Ce récepteur agit comme un radar ultra-précis qui reconnaît des protéines spécifiques présentes à la surface des cellules cancéreuses, notamment la protéine CD19 fréquemment exprimée dans les leucémies et lymphomes. Une fois reprogrammées, ces cellules sont multipliées en laboratoire pour atteindre plusieurs millions d'exemplaires avant d'être réinjectées au patient. Les principales étapes du traitement comprennent :
- Le prélèvement des lymphocytes T par aphérèse
- La modification génétique en laboratoire pour ajouter le récepteur CAR
- La multiplication des cellules modifiées pendant 2 à 4 semaines
- Une chimiothérapie préparatoire pour éliminer les cellules immunitaires existantes
- La perfusion des cellules CAR-T au patient
Taux de rémission complète atteignant 80% chez certains patients pédiatriques
Les résultats cliniques des thérapies CAR-T sont spectaculaires, particulièrement chez les enfants atteints de leucémie lymphoblastique aiguë. Les essais cliniques montrent des taux de rémission complète pouvant atteindre 80% chez les jeunes patients qui n'avaient plus d'options thérapeutiques. Ces chiffres contrastent fortement avec les taux de survie historiques pour ces cancers en rechute. Par ailleurs, plusieurs traitements CAR-T ont obtenu des autorisations de mise sur le marché, notamment le tisagenlecleucel et l'axicabtagene ciloleucel. Néanmoins, ces thérapies peuvent provoquer des effets secondaires importants comme le syndrome de relargage cytokinique, qui nécessite une surveillance médicale étroite. Malgré ces défis, les thérapies CAR-T transforment radicalement le pronostic de nombreux patients considérés comme incurables.
Les vaccins thérapeutiques personnalisés adaptés au profil tumoral de chaque patient
Les vaccins thérapeutiques personnalisés représentent une approche révolutionnaire dans le traitement du cancer. Contrairement aux vaccins préventifs traditionnels, ces vaccins visent à stimuler le système immunitaire pour qu'il reconnaisse et attaque les cellules cancéreuses déjà présentes dans l'organisme. Chaque vaccin est conçu spécifiquement pour un patient donné, en fonction des caractéristiques uniques de sa tumeur. Cette personnalisation maximale permet d'obtenir une réponse immunitaire ciblée et puissante. Par ailleurs, cette approche réduit considérablement les risques d'effets secondaires comparés aux traitements conventionnels. Les chercheurs développent ces vaccins en identifiant les mutations spécifiques présentes dans les cellules tumorales de chaque patient. Ensuite, ils créent un vaccin contenant des antigènes correspondant à ces mutations particulières.

- Traitement immunothérapeutique sur mesure conçu selon les mutations tumorales individuelles
L'analyse génomique pour créer des vaccins sur mesure contre les néoantigènes
L'analyse génomique constitue le fondement de cette approche personnalisée. Les scientifiques séquencent l'ADN de la tumeur et le comparent à celui des cellules saines du patient. Cette comparaison révèle les néoantigènes, ces protéines anormales produites uniquement par les cellules cancéreuses. Le processus comprend plusieurs étapes essentielles :
- Prélèvement d'un échantillon de la tumeur et de tissu sain
- Séquençage génétique complet pour identifier les mutations tumorales
- Sélection des néoantigènes les plus susceptibles de déclencher une réponse immunitaire
- Fabrication du vaccin personnalisé contenant ces antigènes spécifiques
- Administration au patient pour stimuler son système immunitaire
Cette technologie avancée nécessite généralement entre 8 et 12 semaines pour produire un vaccin complet. Cependant, les progrès technologiques permettent de réduire progressivement ce délai. De plus, l'intelligence artificielle aide désormais à prédire quels néoantigènes seront les plus efficaces pour chaque patient.
Résultats cliniques prometteurs dans les cancers du pancréas et du poumon
Les essais cliniques montrent des résultats encourageants pour ces vaccins personnalisés. Dans le cancer du pancréas, l'un des plus difficiles à traiter, certains patients ont vu leur tumeur se stabiliser ou régresser. Des études récentes démontrent que les patients vaccinés présentent une activation significative de leurs lymphocytes T spécifiques contre la tumeur. Par conséquent, leur système immunitaire devient capable de reconnaître et d'éliminer les cellules cancéreuses de manière durable. Pour le cancer du poumon, les résultats s'avèrent également prometteurs avec une amélioration notable de la survie sans progression. Néanmoins, ces traitements restent encore principalement disponibles dans le cadre d'essais cliniques. Finalement, les chercheurs travaillent activement à rendre cette technologie plus accessible et abordable pour tous les patients.
Les virus oncolytiques qui détruisent sélectivement les tumeurs
Les virus oncolytiques représentent une approche innovante dans le combat contre le cancer. Ces virus modifiés en laboratoire possèdent une capacité unique : ils infectent et détruisent spécifiquement les cellules cancéreuses tout en épargnant les tissus sains. Contrairement aux traitements traditionnels, cette stratégie exploite les faiblesses naturelles des tumeurs. En effet, les cellules cancéreuses présentent souvent des défenses antivirales affaiblies, ce qui les rend particulièrement vulnérables à ces agents thérapeutiques. D'ailleurs, plusieurs virus oncolytiques font actuellement l'objet d'études cliniques approfondies, démontrant des résultats encourageants chez des patients atteints de cancers avancés.
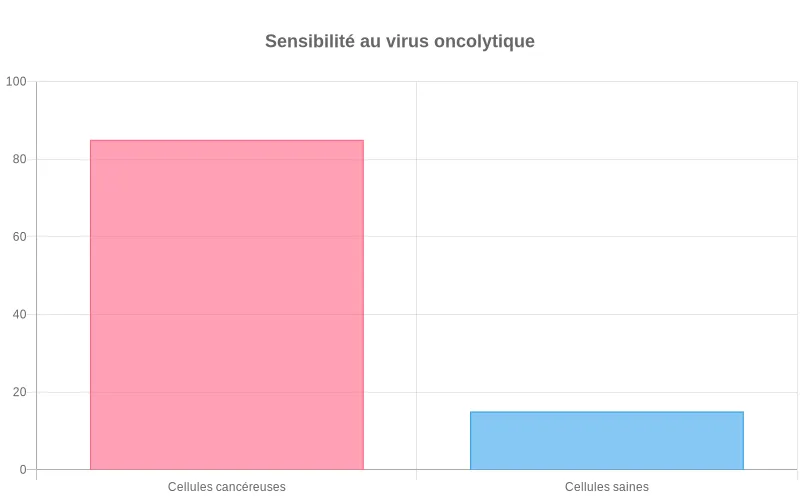
Le T-VEC et les nouveaux virus modifiés pour infecter uniquement les cellules cancéreuses
Le talimogène laherparepvec, communément appelé T-VEC, constitue le premier virus oncolytique approuvé pour le traitement du mélanome. Ce virus dérive du virus de l'herpès simplex de type 1, modifié génétiquement pour cibler exclusivement les cellules tumorales. Par conséquent, le T-VEC s'injecte directement dans les lésions cutanées accessibles où il se réplique activement. Au-delà du T-VEC, les chercheurs développent actuellement de nouveaux virus oncolytiques basés sur différentes souches virales. Ces nouveaux candidats incluent des adénovirus, des réovirus et des virus de la vaccine, chacun présentant des avantages spécifiques selon le type de cancer traité. Néanmoins, tous partagent un principe commun : leur capacité à distinguer les cellules malignes des cellules normales grâce à des modifications génétiques précises.
| Type de virus | Origine virale | Cancers ciblés |
|---|---|---|
| T-VEC | Herpès simplex | Mélanome |
| ONYX-015 | Adénovirus | Tumeurs solides |
| Reolysin | Réovirus | Cancers colorectaux |
Double action antitumorale : lyse virale et stimulation de la réponse immunitaire systémique
L'efficacité des virus oncolytiques repose sur un mécanisme d'action double particulièrement puissant. Premièrement, ils provoquent la lyse directe des cellules cancéreuses. Lors de leur réplication à l'intérieur de la tumeur, les virus accumulent de nouvelles particules virales jusqu'à ce que la cellule éclate littéralement. Deuxièmement, cette destruction cellulaire libère des antigènes tumoraux et des signaux de danger qui alertent le système immunitaire. Ainsi, les cellules immunitaires du patient, notamment les lymphocytes T et les cellules dendritiques, reconnaissent ces signaux et déclenchent une réponse antitumorale généralisée. Cette activation immunitaire présente plusieurs avantages majeurs :
- Elle permet d'atteindre des métastases distantes non infectées par le virus
- Elle crée une mémoire immunitaire durable contre la tumeur
- Elle réduit les risques de récidive à long terme
- Elle peut être combinée avec d'autres immunothérapies pour amplifier l'effet thérapeutique
Finalement, cette double action transforme la tumeur en véritable usine à vaccins personnalisés, enseignant au système immunitaire comment reconnaître et éliminer les cellules cancéreuses dans tout l'organisme.
Les combinaisons thérapeutiques qui multiplient l'efficacité des traitements
L'une des avancées majeures en immunothérapie réside dans l'association de plusieurs traitements. Les chercheurs ont découvert que combiner différentes approches permet d'obtenir des résultats bien supérieurs à ceux d'une monothérapie. Cette stratégie repose sur un principe simple : attaquer le cancer sur plusieurs fronts simultanément pour empêcher les cellules tumorales de développer des mécanismes de résistance. Les protocoles combinés activent également différentes branches du système immunitaire, créant ainsi une réponse antitumorale plus complète et durable.

- Association de traitements médicaux pour décupler les résultats cliniques et améliorer la santé
Association immunothérapie et chimiothérapie pour potentialiser les résultats
L'association entre immunothérapie et chimiothérapie représente une révolution thérapeutique. Contrairement aux idées reçues, la chimiothérapie ne se contente pas de détruire les cellules cancéreuses. Elle provoque également leur mort immunogène, libérant des antigènes tumoraux qui stimulent le système immunitaire. Lorsqu'on ajoute une immunothérapie à ce processus, les lymphocytes T deviennent plus efficaces pour reconnaître et éliminer les cellules malignes. Cette synergie s'observe particulièrement dans les cancers du poumon, où cette combinaison est devenue un standard de soin. Les bénéfices incluent :
- Une réduction plus rapide de la taille des tumeurs
- Une amélioration du taux de réponse objective
- Un contrôle prolongé de la maladie
- Une meilleure qualité de vie pour les patients
| Type de combinaison | Cancer ciblé | Amélioration de survie |
|---|---|---|
| Immunothérapie + chimiothérapie | Poumon non à petites cellules | +6 à 8 mois |
| Double immunothérapie | Mélanome avancé | +12 à 15 mois |
| Immunothérapie + thérapie ciblée | Rein métastatique | +10 à 14 mois |
Gains de survie globale dépassant 12 mois dans les essais cliniques récents
Les données cliniques confirment l'impact spectaculaire des combinaisons thérapeutiques. Dans plusieurs essais de phase III, les patients traités par association ont bénéficié d'un gain de survie globale dépassant largement les 12 mois comparativement aux traitements standards. Ces résultats exceptionnels s'accompagnent d'une augmentation significative du taux de survie à cinq ans, transformant certains cancers métastatiques en maladies chroniques contrôlables. Par ailleurs, les protocoles combinés permettent parfois de réduire les doses de chimiothérapie, diminuant ainsi les effets secondaires tout en maintenant une efficacité optimale.




